- INÍCIO
- CINÉTICA QUÍMICA E EXERCÍCIOS RESOLVIDOS
- CÁLCULO ESTEQUIOMÉTRICO
- LINKS SOBRE QUIMICA AMBIENTAL E OUTROS TÓPICOS
- EXERCÍCIOS DE TERMOQUÍMICA
- ISOMERIA E MEDICAMENTOS
- RADIOQUÍMICA EXERCÍCIOS RESOLVIDOS
- PROPRIEDADES DA MATÉRIA
- QUÍMICA ORGÂNICA
- TOXINA DESCOBERTA CAUSA MEDO EM PESQUISADORES....
- SITES DAS UNIVERSIDADES, SEU FUTURO...
- TESTE VOCACIONAL
- LITERATURA INFANTO JUVENIL
- FOTOS DOS MEUS ALUNOS ( ENVIE SUAS FOTOS)
- DEIXAR PERGUNTA?
- Contactos
ISOMERIA E MEDICAMENTOS

É fato que os isômeros são tão parecidos que muitas vezes são confundidos, o que pode ser trágico em se tratando da saúde. Foi exatamente o que ocorreu na Europa na década de 1960, com o lançamento de um medicamento com efeito tranquilizante e sonífero nomeado de Talidomida. As gestantes da época procuraram por este efeito calmante sem ter ideia do que poderia ocorrer ao feto em gestação. Foi então que se registrou o nascimento de bebês com membros atrofiados (mãos, pés, pernas). Esse efeito teratogênico foi resultado do uso da Talidomida.
A talidomida apresenta dois isômeros:
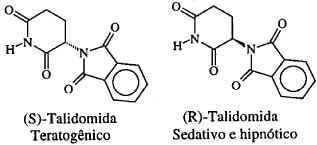
(S) talidomida → teratogênica
(R) talidomida → efeito tranquilizante
Como vemos, a substância Talidomida, dependendo do isômero usado, produz efeitos completamente diferentes em nosso organismo, daí a importância do estudo da isomeria respectiva. A diferença pode ser percebida através das estruturas:
Isômeros óticos da Talidomida: uma simples mudança no posicionamento do N (nitrogênio central - um para frente e outro para trás) difere as duas estruturas.
A partir daí a mistura racêmica (presença de isômeros) dos medicamentos sintéticos foi banida pela Indústria farmacêutica. Desde então se aprimorou a produção de medicamentos quirais, que têm em sua estrutura os átomos (na maioria carbonos) com orientação tridimensional bem definida. Uma modificação dessa orientação ocasiona a diminuição ou mudanças nos efeitos biológicos, como ocorreu no caso da Talidomida
No Brasil, a talidomida foi fortemente retirada de circulação somente em 1964. Em 1994, foi publicada a portaria nº 63, da Secretaria de Vigilância Sanitária do Ministério da Saúde, proibindo o uso da talidomida por mulheres em idade fértil. Em 1997, foi publicada a portaria nº 354, do Ministério da Saúde, que regulamenta o registro, a produção, a fabricação, a comercialização, a prescrição e a dispensação de produtos à base de talidomida, aplicados no tratamento de complicações de doenças como Aids, lúpus, mieloma múltiplo e hanseníase. Também nestes casos, o uso de tais produtos é proibido para mulheres em idade fértil.
https://qnint.sbq.org.br/qni/visualizarConceito.php?idConceito=19
A Estereoisomeria E A Tecnologia Industrial De Separação Da Bupivacaína No Mundo
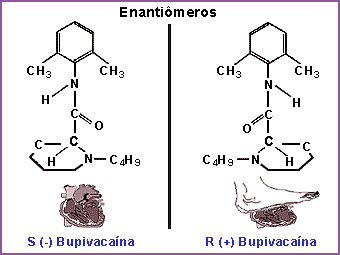
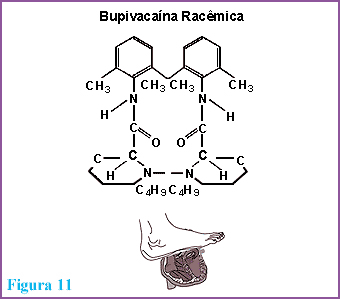
Com o advento da tecnologia de resolução (separação dos isômeros ópticos numa mistura racêmica) em escala industrial, foi possível a comercialização do primeiro anestésico local isómerico, a ropivacaína. Por suas propriedades físico-químicas, conferidas pelo radical propil ligado ao esqueleto pipecolilxilidida, este anestésico local exibe características farmacológicas próprias. Em termos de atividade bloqueadora de nervo, avaliada com doses equipotentes, a ropivacaína mostrou ser menos potente que a bupivacaína racêmica, porém significativamente menos depressora quanto à cardiotoxicidade potencial9. Em razão deste perfil farmacológico e com embasamento nos resultados obtidos com o isômero levógiro da bupivacaína através da experimentação pré-clínica (que evidenciam uma menor propensão para a toxicidade cardíaca mas com potência bloqueadora de nervo semelhante a forma racêmica), a industria farmacêutica se lançou na estratégia de preparação da levobupivacaína, descontaminando-a do componente cardiodepressor, o isômero dextrógiro24. O Reino Unido e o Brasil estão adotando esta tecnologia de última geração, individualmente, e as pesquisas estão nas fases avançadas da investigação clínica nestes países (Figuras 10 e 11).
A primeira e a mais contundente advertência para a importância da estereoisomeria foi feito por Äriens5, ao alertar os pesquisadores de que a desconsideração com a estereoisomeria na pesquisa médica seria uma sofisticada falta de senso na farmacologia clínica e farmacocinética. Ruffolo6, por sua vez, vem conclamando os órgãos governamentais reguladores (no Bra, Secretaria de Vigilância Sanitária do Ministério da Saúde) a não permitir o licenciamento de medicamentos novos que não sejam moléculas isoméricas puras, a menos que razões médicas justifiquem a existência da forma racêmica.
Paripasso com esta conscientização estereoisomérica, começou a se formar a parceria da indústria farmacêutica com a medicina em geral e a anestesiologia em particular.
Cerca de 82% dos medicamentos utilizados na Terapêutica Clínica, são compostos quirálicos e apresentados sob a forma racêmica, segundo Manson24, enquanto Calvey13 listou os agentes quirálicos e aquirálicos utilizados na prática anestesiológica13 (Quadro I).
|
QUADRO I |
||
|
Aquirálicos |
Quirálicos |
Quirálicos |
|
Propofol |
Etomidato |
Tiopental |
|
Óxido Nitroso |
Ropivacaína |
Metohexital |
|
Cloprocaína |
Tubocurarina |
Cetamina |
|
Lidocaína |
Morfina |
Halotano |
|
Tetracaína |
Hioscina |
Enflurano |
|
Galamina |
Alcurônio |
Isoflurano |
|
Fentanil |
|
Prilocaína |
|
Petidina |
|
Mepivacaína |
|
Neostigmina |
|
Bupivacaína |
|
Edofrônio |
|
Etidocaína |
|
Dopamina |
|
Atropina |
|
Sevoflurano |
|
Dobutamina |
|
|
|
Glicopirrolato |
A relação custo/benefício favorável na obtenção de isômeros puros se baseia nas vantagens expressivas que esta tecnologia de separação de irmãos gêmeos trará para a racionalização terapêutica. Se não vejamos: ropivacaína, levobupivacaína (já discutidas); prilocaína, cujo enantiômero R(-) é mais rapidamente metabolizado, produzindo uma concentração plasmática mais alta de ambas: o-toluídina e metahemoglobina); cetamina: a indução da reação de emergência psíquica manifestada com este agente se deve ao isômero R(-) cetamina; verapamil: que se encontra na fase de resolução visando a eliminação da depressão da velocidade de condução cardíaca, promove este efeito colateral indesejável devido ao isômero levógiro13.
Concluindo e parafraseando Manson25 que invocou a filosofia dos Mestres Zen, (bater palmas com uma única mão, associando-a à estereoisomeria), este conceito figurativo, merece ser visto como o modelo para a síntese industrial de novos compostos medicamentosos, e que seguramente se constituirá numa realidade para este segundo milênio, em termos de racionalização terapêutica.
,
OBSERVAÇÕES: E COMENTÁRIOS
OS REMÉDIOS
CONTEÚDO: ISOMERIA ESPACIAL OU ESTÉREOISOMERIA
HABILIDADES: RELACIONAR A ISOMERIA ÓPTICA E GEOMÉTRICA COM AS PROPRIEDADES INTRÍSECAS DOS MEDICAMENTOOS E OUTRAS SUBSTÂNCIAS.
Ufpa-2001
A talidomida, sintetizada pela primeira vez na forma racêmica, na Alemanha em 1954, é uma substância dotada de propriedades químicas capazes de controlar ansiedade, tensão nervosa e náuseas. Em 1960, foram descobertos seus efeitos teratogênicos. Os estudos demonstraram que gestantes que consumiram essa substância geraram fetos com má formação e que o causador dessa anomalia é o isômero l-talidomida.
Admitindo que 4mg de l-talidomida seja a dose mínima capaz de provocar a má formação do feto, explique se o fato de uma gestante consumir um medicamento cuja fórmula contenha 12mg de talidomida racêmica poderá ocasionar má formação do feto.
Ufpa- 2003
A bula de um medicamento
A atividade biológica do medicamento é devido ao isômero dextrógiro de uma substância A, enquanto que o isômero levógiro é inativo.
Cada drágea contém 5,0 mg do isômero dextrógiro da substância A.
O isômero levógiro não é empregado na composição do medicamento.
Processadas as análises físicas e químicas de um lote deste medicamento, observou-se que cada drágea continha 5,0 mg da substância A que revelou rotação ótica igual a zero.
a) O medicamento analisado, está adulterado? Justifique.
b) Quantos miligramas do isômero destrógiro contém uma drágea da substância A, analisada.
Isomeria
Definição: É o fenômeno no qual dois ou mais compostos diferentes, apresentam a mesma fórmula molecular.
Exemplos: CH3 - CH2 - OH CH3 - O - CH3
Isomeria espacial ou estéreoisomeria ou estéreoquimica
Observações importantes
Obs1: A estéreoquimica é a parte da química que estuda as moléculas químicas em três dimensões.
Obs2: As proteínas, são compostos químicos, essenciais ao todo funcionamento do organismo humano e apresentam estrutura tridimensional.
Obs3: As enzimas, que são proteínas, são produzidas no corpo humano, para catalisarem (encaixarem) em um único substrato. (Sistema chave e fechadura)
Tipos de estéreoisomeria
ISOMERIA ÓPTICA:
1- Definição:
È o fenômeno em que um composto tem a capacidade de desviar o plano da luz polarizada.
LUZ POLARIZADA: É a luz cujas ondas eletromagnéticas apresentam um único plano de vibração.
2- Classificação dos isômeros ópticos:
2.1- Isômero Destrógiro (d ou +). É aquele que promove o desvio do plano da luz polarizada para direita.
O destrógiro é um isômero ativo
2.2- Isômero Levógiro (l ou -). É aquele que promove o desvio do plano da luz polarizada para esquerda.
O levógiro é um isômero ativo
I M P O R T A N T E !
A mistura racêmica (forma racêmica ou racemato) é a mistura equimolecular de isômeros destrógiros e levógoros, ou seja, uma mistura onde 50% das moléculas representam um isômero destrógiros e 50% representam um isômero um isômero levógiro, ocorrendo compensação intermolecular (compensação externa).Logo o racemato é inativo, ou seja não promove desvio no plano de vibração da luz polarizada.
Nota: Existem, para os isômeros ópticos, dois tipos de atividade. A primeira é a atividade óptica e a segunda é a atividade biológica. A atividade biológica dos isômeros é a ação dos mesmos no organismo, semelhantes aos medicamentos. Nem sempre para atividade biológica os isômeros serão ativos, porém, para a atividade óptica, serão sempre ativos.
Espelho
Veja a seguir uma série de propriedades fisiológicas diferentes dos isômeros ópticos.
Isômeros ópticos X hormônio.
A adrenalina ou epinefrina posui um centro quiral, logo são possíveis dois isômeros ópticos, mas apenas um deles possui efeito fisiológico no nosso organismo ( acelera os batimentos cardíacos numa situação de stress )
Isômeros ópticos X Sabores.
O aspartame possui dois carbonos assimétricos, sendo possíveis quatro isômeros ópticos,sendo dois deles de sabor doce e dois de sabor amargo.
Isômeros ópticos X metabolismo
A glicose destrógira tem participação fundamental no metabolimo das células humanas, entretanto a glicose levógira não participa do metabolismo.
Isômeros ópticos X fragrâncias
O Limoneno possui um carbono quiral, logo apresenta dois isômeros ópticos.Um deles é responsável pela fragância de limão e o outro pela fragrância de laranja
Isômeros ópticos X medicamentos
O Naproxeno possui um carbono quiral, logo apresenta dois isômeros ópticos. Um deles tem ação antiflamatória e o outro causa danos ao fígados
IMPORTANTE!
FÁRMACOS E QUIRALIDADE
Fármacos quirais (que apresentam isomeria óptica) tem em sua estrutura um ou mais átomos com orientação tridimensional muito bem definida.A modificação dessa orientação pode levar á diminuição do efeito biológico, à sua total supressão ou ao aparecimento de um efeito biológico adverso.
Nota: No mercado mundial existem vários fármacos que já são vendidos nas farmácias em suas formas opticamente puras, ou seja, sem a mistura com o outro isômero que não tem atividade biológica.
A venda de fármacos na forma de mistura racêmica ainda ocorre. Entretanto, é necessário saber qual é o estéreoisômero responsável pela atividade biológica adversa e ter absoluta certeza que o estéreoisômero inativo, presente na mistura, não tem nenhuma atividade biológica adversa.
Desvantagem dos fármacos em seu uso na forma racêmica
1- A dose a ser utilizada deve ser aumentada, pois somente metade tem efeito farmacológico desejado;
2- O paciente ingere, a cada dose do fármaco, 50% de uma substância química desnecessária ( isômero inativo )
3- A outra metade do fármaco , que é inativo, pode agir como um corpo estranho no organismo , podendo causar várias alterações no organismo. Foi o caso da síndrome da talidomida.
PARA SABER MAIS...
MEDICAMENTOS GENÉRICOS.
A adoção do uso dos medicamentos genéricos é favorável aos interesses da população e a saúde pública, constituindo um passo inicial e essencial para a efetiva implementação de ações capazes de promover a melhoria das condições da assistência á saúde e acesso aos medicamentos.
O grande custo dos laboratórios consiste mais na propaganda e menos no princípio ativo.
A "denominação Genérica" é simplesmente o nome do principio ativo do fármaco.
Os médicos ainda hesitam em prescrever pelo nome genérico, por hábito cultural, sedimentado pelo intenso assédio promovido pela indústria farmacêutica que vinculam uma literatura de fantasia ou comercial.Por exemplo:
O Flanax, que é um antiflamatório, é o nome comercial que é vinculado nas propagandas de televisão. O nome do princípio ativo é Naproxeno.















